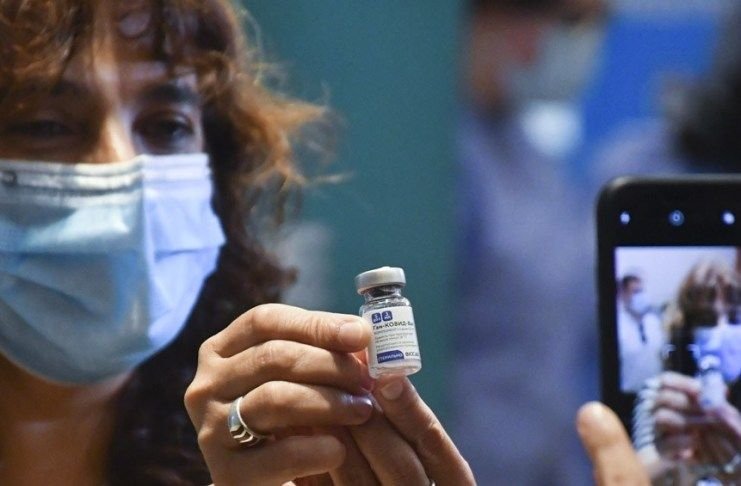
Las reacciones reportadas tras la aplicación de la vacuna Sputnik V contra el coronavirus «fueron leves y moderadas, no requirieron hospitalización y están dentro de los parámetros normales de cualquier vacuna», dijeron voceros del Ministerio de Salud a pocos días del inicio de la campaña de inmunización.
La cartera sanitaria informó que hubo 317 casos de reacciones leves posteriores a la vacunación, tras la aplicación de 32.013 dosis de la rusa Sputnik V entre personal de salud en Argentina, las cuales fueron reportadas en el Registro Federal de Vacunación Nominalizado (NoMiVac).
Fuentes del Ministerio de Salud dijeron que la elaboración de este tipo de estudios estaba previsto dentro de la planificación estratégica para el seguimiento de los eventos relacionados con la inmunización.
Este tipo de registros y controles «está planificado y pensado en el plan estratégico, y hay un sistema de registro en el Sistema Nacional de Vigilancia. Lo que se hizo, en este caso, es instar a las jurisdicciones y a los ámbitos de vacunación a que registraran eventos como dolores en el sitio de vacunación, febrícula, fiebre o dolor muscular», añadieron.
Por último, explicaron que hasta ahora, «los registros en Argentina son coincidentes con los ensayos de fase 1 y 2 de Rusia» y que «los efectos adversos adversos son los esperados».
Agregaron que esos efectos adversos leves mencionados «aparecen dentro de las 24 horas de aplicación de la vacuna y desaparecen entre las 24 y 48 horas posteriores a la aplicación».
Las distribución de las 300 mil dosis de la vacuna Sputnik V en el país concluyó el pasado lunes 28, en una campaña que requirió tareas ininterrumpidas durante 24 horas y la utilización de cientos de conservadoras, toneladas de hielo seco y un gran número de camiones para iniciar mañana un histórico esquema de vacunación de miles de trabajadores de la salud en todas las provincias.
En el marco de un diseño «federal, equitativo y proporcional» de asignación de las dosis a cada provincia, el plan de vacunación se inició el martes 29 de diciembre y, en forma simultánea, cada jurisdicción comenzó a desarrollar el proceso bajo un plan propio de aplicación de las dosis.
El mismo día del inicio de las aplicaciones, la directora de Evaluación y Registros de Medicamentos de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (Anmat), Agustina Bisio, aseguró que la documentación referida a la Sputnik V que recibió el organismo «es tan detallada como la de las otras investigaciones», y sostuvo que «las otras vacunas que están siendo autorizadas en el mundo tienen más incidencias de eventos adversos» que la desarrollada por Rusia.